Les résultats d’Hemgenix sur une période de 4 ans en confirment la constance

MONTRÉAL, le 12 mars 2025 – Les résultats de l’étude HOPE-B sur la thérapie génique pour l’hémophilie B Hemgenix font état d’une constance dans l’expression du facteur IX (FIX) quatre ans après son administration.
Le Dr Steven Pipe, du Programme sur l’hémophilie et des troubles de la coagulation de l’Université du Michigan, a présenté les résultats après 48 mois à l’occasion du Congrès de l’Association européenne pour l’hémophilie et les troubles connexes (ou EAHAD, pour European Association of Haemophilia and Allied Disorders) à Milan, en Italie, en février.
Le taux moyen de FIX chez les 54 sujets de l’étude 48 mois après le traitement était de 37,4 %, pour ainsi dire inchangé par rapport aux résultats obtenus après 36 mois, témoignant d’une constance très prometteuse à long terme.
Le tableau ci-dessous montre les différentes intensités de l’hémophilie B et les taux de FIX obtenus chez les 54 participants.
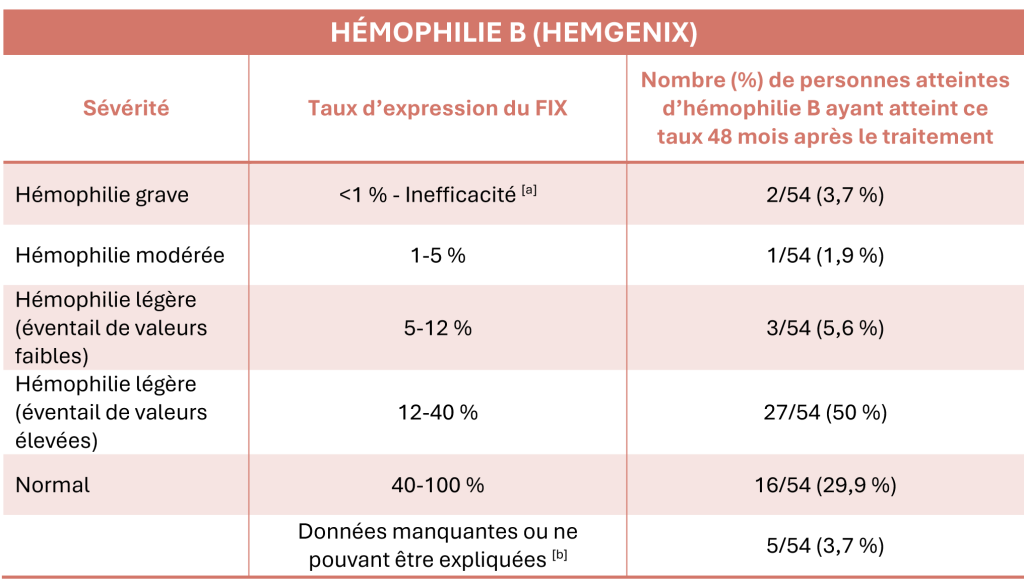
[a] Inefficacité de la thérapie génique en l’absence de signes d’importation et d’expression du gène du facteur IX.
[b] Les dernières données sur l’activité du facteur IX sont manquantes chez 5 patients : un participant de 77 ans en raison de son décès (non lié à l’étranacogène dézaparvovec) 15 mois après la thérapie génique; un autre à la suite d’une transplantation hépatique; un troisième après que le patient soit revenu à la prophylaxie par le FIX; et deux autres dont les derniers dosages de facteur IX disponibles remontaient à 42 mois.
Le traitement n’a eu aucun effet sur l’expression du FIX chez deux sujets; l’un est retourné à la prophylaxie continue par FIX au cours de la 3e année (relaté précédemment), et aucun n’a repris la prophylaxie au cours de la 4e année.
Soixante pour cent (60 %, 31/54) des participants n’ont manifesté aucun saignement articulaire pendant la période de quatre ans suivant le traitement; 46,3 % (25/54) n’ont reçu aucune perfusion de FIX pendant ce temps.
Aucun cas de génotoxicité associé au VAA5 n’a été confirmé, et on n’a observé aucune hépatotoxicité persistante. Le VAA5 est le vecteur viral utilisé pour acheminer le gène du FIX au foie.
Hemgenix a été approuvé par Santé Canada en octobre 2023. L’Agence des médicaments du Canada (anciennement, l’ACMTS) a formulé une recommandation positive concernant son remboursement en juin 2024, selon les négociations tarifaires. Au Québec, l’INESSS a formulé une recommandation négative. Le fabricant, CSL Behring Canada, et l’Alliance pharmaceutique pancanadienne (APP), au nom des régimes publics canadiens d’assurance médicaments, ont entamé les négociations tarifaires en août 2024. De telles négociations s’étalent généralement sur une période de six mois.
Pour plus de renseignements, consulter le Programme d’éducation à la thérapie génique de la SCH, à l’adresse www.hemophilia.ca/fr/therapie-genique.